Klavulánsav, oxapenamok
Felfedezés, természetes származékok
1967-ben az angol Beecham cég egy olyan kutatási programba kezdett, amelyben gombák és aktinomicéták körében β-laktamáz enzimgátló hatást mutató anyagok iránt nyomoztak. Módszerük az volt, hogy a vizsgálandó mintákat olyan agar lemezre vitték rá, amely benzil-penicillint és β-laktamázt termelő Klebsiella aerogenes-t tartalmazott. Enzimgátló hatás esetén inkubálás után a felvitel helye körül inhibíciós zóna látszott, mivel a benzilpenicillin így már képes volt gátolni a baktériumok szaporodását. Egy Streptomyces clavuligerus törzs esetén tapasztaltak erős gátló hatást. Az anyagról a biokromatográfiás elővizsgálatok során már kiderült, hogy nem azonos a Streptomyces olivacius termelte hasonló hatású anyagokkal, és az MM 14151 ill. a klavulánsav triviális nevet kapta. Meglepetésre egy egészen újszerű β-laktám vázas vegyületnek bizonyult, mivel:
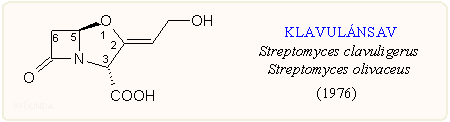
- a kénatom helyett oxigént tartalmaz a heterogyűrűben;
- a β-laktám gyűrűhöz nem kapcsolódik acilamino oldallánc;
- az oxazolidin gyűrűn egy β-hidroxietilidén szubsztituens van.
A klavulán sav szabályos kémiai neve Z-(2R,5R)-3-(β-hidroxietilidén)-7-oxo-4-oxa-1-azabiciklo[3.2.0]heptán-2-karbonsav, s az alapváz a penicillinek mintájára a klavám triviális nevet kapta. E szerkezeti különlegességen túlmenően a klavulánsav biológiai aktivitása is eltér a "szokásos" képtől, amennyiben csak gyenge antibakteriális hatást mutat, viszont potens β-laktamáz enzimgátló sajátsággal rendelkezik, amint ezt az arról szóló fejezetben tárgyaljuk.
A klavulánsavat termelő Streptomyces clavuligerus micéliumából még két származékot izoláltak, a klavaminsavat és proklavaminsavat; mindkettő a klavulánsav prekurzorja a bioszintézis során:
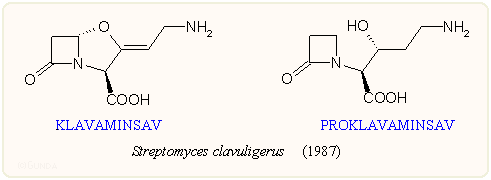
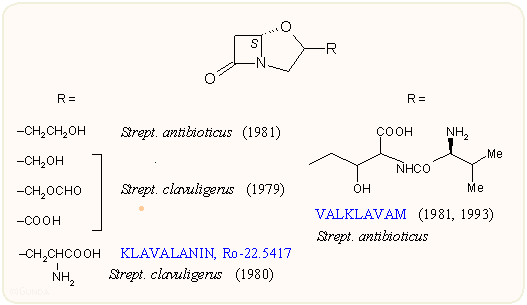
A különböző Streptomyces-ekben több másfajta klavámvázas vegyületet is találtak. Ezekre egységesen jellemző, hogy a két gyűrű kapcsolódásánál a C-5 atom konfigurációja a klavulánsavval ellentétben S. A biológiai hatás is teljesen eltérő: a β-laktamáz enzimmel a vegyületek nem lépnek kölcsönhatásba, viszont kifejezett gombaellenes hatásuk van. Bakteriosztatikus hatást csak metionin hiányos táptalajon mutatnak, így valószínűleg a metionin bioszintézisébe avatkoznak be. Különösebb jelentőségük nincs.
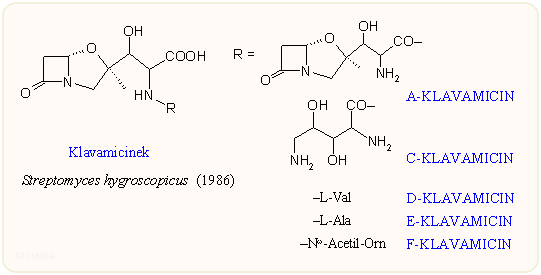
A Sandoz kutatói által előszőr leírt klavamicinek sem tartalmazzák a 3-as helyzetben "kötelező" karboxil csoportot, s peptidszerű oldalláncuk van; az A-klavamicin két klavám egységet tartalmaz. A vegyületek Candida speciesek ellen kifejezett, bár a gyakorlati alkalmazáshoz elégtelen gombaellenes hatást mutatnak.
A klavulánsav bioszintézisét külön fejezetben ismertetjük.
Kémiai tulajdonságok
A klavulánsav β-laktám gyűrűje protikus oldószerekben a penicillinekéhez hasonlóan érzékeny bázisokra. Nemvizes közegben, elsősorban az észtereknél bázisok hatására más folyamat játszódik le, nevezetesen az exociklikus kettőskötés vándorlása és az O—C(5) kötés hasadása következik be. Ez utóbbi általában megfordítható, ill. egyensúlyi folyamat.
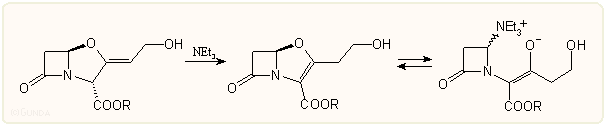
Hasonló folyamat játszódhat le piridin, metanol stb. hatására, sőt melegítésre is: pl az alábbi származék 80 °C-on megfelelő dipolarofil jelenlétében triciklikus származékká alakul, ami úgy magyarázható, hogy az először keletkezett immónium származék malonát oldallánca tautomerizálódik azometin-iliddé.
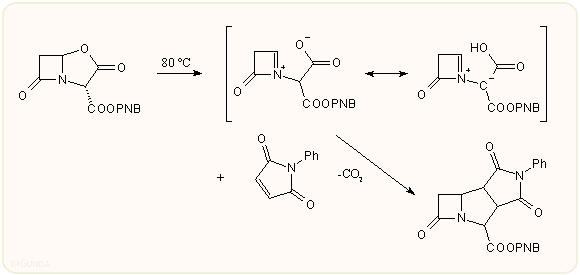
Gyakorlati szempontból igen jelentős az allilos hidroxil csoport továbbalakíthatósága: észterezhető, halogénezhető, oxidálható s ez sok helyettesített új származék elkészítését teszi lehetővé. Néhány ilyen reakciót a következő ábra foglalja össze. Ezeknek a származékoknak nagy része a klavulánsavhoz hasonlóan jó β-laktamáz gátló hatással rendelkezik.
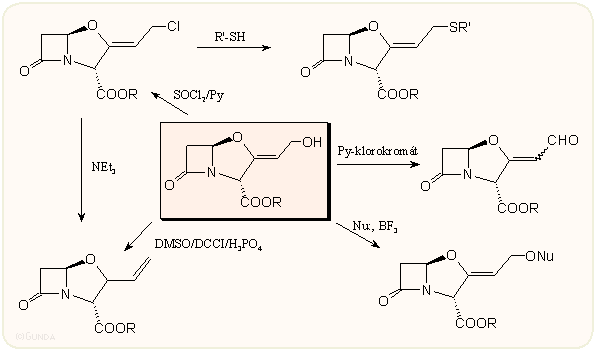
A klavulánsav totálszintézisére több közelítés ismert. Bentley és mtsai eljárása 4-metiltio-azetidinonból indul, amelyből a megfelelő N-szubsztituens kialakítása után a β-laktám kémiában ismert módon egy labilis klórszármazékot készít s ezt használja gyűrűzárásra, eredményül a (±)-klavulánsav metilészterét kapja:
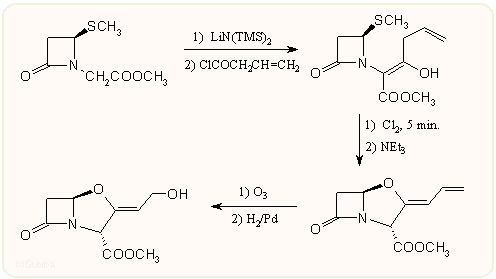
Ennek a szintézisnek több variációját kidolgozták, főleg 2-es helyzetben szubsztituált analógok előállítása végett, a 4-SMe vagy 4-SC6H5-azetidinont többnyire 4-acetoxi-azetidinonból állítják elő közvetlen nukleofil cserével. Ez utóbbiból közvetlenül is el lehet jutni a klavám vázhoz, bár ez nem annyira kedvező módszer:
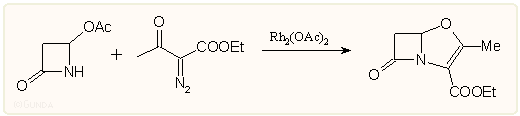
A további telítetlen klavám vázanalógok tulajdonképpen oxapenem származéknak is nevezhetők. A karbapenemekre jellemző 6-os hidroxi tartalmú vagy fluor analóg oldalláncot tartalmazók mind antibakteriálisan, mint laktamáz enzimgátlóként, kombinációban igen hatásosnak bizonyultak A szintézis kulcslépése az S-metil származékból kapott klór vegyület gyűrűzárása az N-oldallánc enol formájával.

Igen érdekes, hogy az analóg módon kapott diasztereomer 5S származék gyakorlatilag azonos hatású a "természetes" 5R származékkal. Ez teljesen elüt az általános tapasztalattól, s feltételezik, hogy itt tk. epimerizálódás játszódik le az C-5 atomon, az oxazolin gyűrű nukleofil miliőben hasonlóképpen felnyílhat, mint ahogy azt a klavulánsavnál láttuk. A 6-os helyzetben penicillinszerű acilamido oldalláncot tartalmazó oxapenemek nem stabilak, oxazolidin származékká rendeződnek át.
Biológiai hatás
Mint már említettük, a klavulánsav csekély antibakteriális hatás mellett jelentős ß-laktamáz enzim gátlással rendelkezik. A különböző baktériumok által termelt különféle β-laktamáz enzimekre gyakorolt hatás természetesen eltérő. Erős gátlás jelentkezik St. aureus és egyéb Gram-pozitív baktériumokból származó laktamázoknál, valamint az II-IV típusú Gram-negatív laktamázoknál. Az I típusú cefalosporinázoknak viszont általában gyenge inhibitora (Enterobacter és Citrobacter törzsek, Pseudomonas aeruginosa, egyes Escherichia coli, Salmonella és Shigella törzsek). Ha a klavulánsavat β-laktamázra érzékeny penicillinekkel kombináljuk, jelentős szinergizmust tapasztalunk: a β-laktamázt termelő baktériumok esetén mintegy "visszatér" az antibiotikum hatása. Az alábbi táblázat mutatja ezt be az amoxicillin esetén.
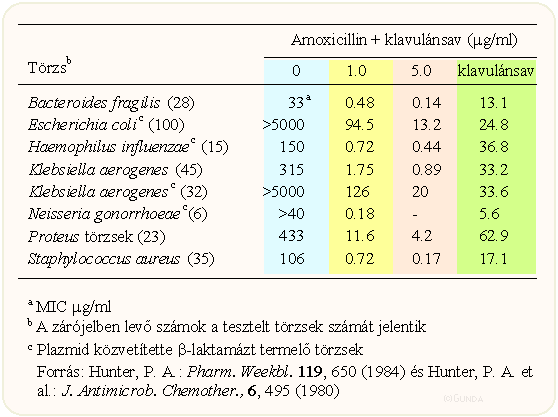
Az alábbi grafikon jobban láttatva mutatja be a szinergizmus felléptét (amoxicillin: piros, klavulánsav: sárga, keverék: zöld):
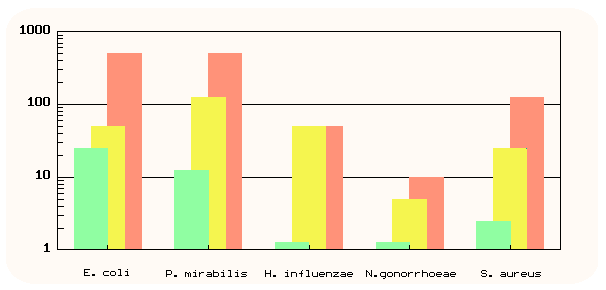
A klavulánsav orálisan is jól felszívódik, a szérumkoncentráció lefutása hasonló az amoxicillinéhez. A kettő kombinációját Augmentin™, Aktil™, stb. néven sok országban forgalmazzák húgyúti, bőrgyógyászati, respirációs fertőzések ellen. A ticarcillin K-só és a klavulánsav kombinációja intravénás felhasználásra Timentin néven kerül forgalmazásra.
A klavulánsavat hatásmechanizmusa alapján az ún. öngyilkos (suicide) típusú inhibitorokhoz sorolják. E. coli TEM-2 β-laktamáz enzim esetén első lépésként az enzim aktív centrumában levő szerin OH csoporttal reagálva alakul ki az első enzim-szubsztrát komplex, amely a β-laktám gyűrű felnyílásával továbbalakul az acilezett enzimmé. Ez vagy még egy ponton reagálva az enzim molekulával azt irreverzibilisen inaktivált enzimmé alakítja, vagy regenerálódik az enzim s felszabadulnak a klavulánsav bomlástermékei:
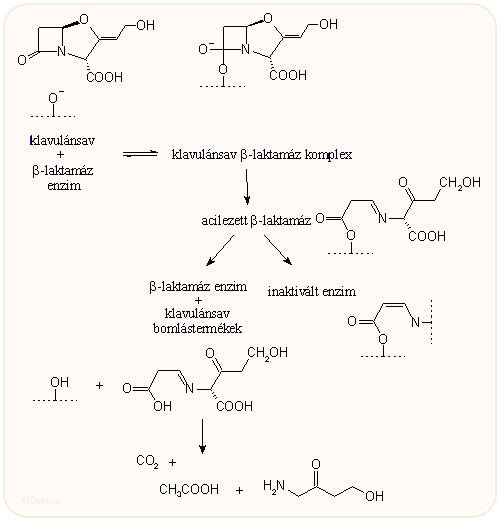
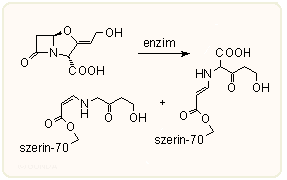
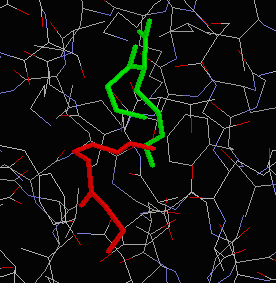
A klavulánsav és Staph. aureus β-laktamáz enzim komplexének röntgendiffrakciós vizsgálatánál kissé más szerkezetű anyagokat lehetett kimutatni. A jobb oldalon a szerin-70-hez kapcsolódott és már elbomlott klavulánsav, valamint egy St. aureus törzsből izolált ß-laktamáz komplexe látható. A klavulánsavból kétféle termék is képződik, valószínüleg ugyanazon az aktív helyen, egymást követő reakciókban. |
|