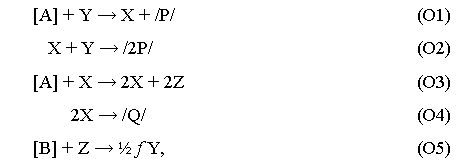
2.1 OszcillációMÉK 1044. oldal:
Az oszcillációs reakciókkal kapcsolatban egyik szótári jelentés sem alkalmazható. Kémia reakciók esetében ugyanis nem beszélhetünk arról, hogy valami „rezeg” vagy „inog”. A kémiai jelenség lényegéhez talán a 3. definíció áll a legközelebb, bár az „erősség” kémiai jelentését nem lenne könnyű megmagyarázni.
A kémiában akkor beszélünk oszcillációról, ha egy kémiai jelenség periodikus.
Mivel egy reakció előrehaladását az abban résztvevő anyagok koncentrációjának időbeli változásával jellemezzük, egy kémiai jelenség periodicitása egyszerűen azt jelzi, hogy bizonyos részecskék koncentrációja időben periodikusan változik. Azaz, a megfelelő koncentráció–idő görbéken – szabályos időközönként – minimumok és maximumok váltják egymást. Az oszcillációt bonyolult berendezések nélkül is érzékelhetjük, ha például egy oldat színe periodikusan változik: piros–kék–piros–kék–stb.
Az oszcilláció bár nem gyakori, de régóta ismert kémiai jelenség. Az egyik legismertebb tankönyvi példa a XVII. századból származik: a foszfor gázfázisú oxidációját vízgőz jelenlétében periodikus felvillanások kísérik (Lengyel, 1967). Az elektrokémiai rendszerek oszcillációs viselkedését már a múlt században megfigyelték. Fechner (1828) gyengén megsavanyított ezüst-nitrát oldatba mártott ezüst- és vaselektródok között áram- és feszültségoszcillációt észlelt. Régóta ismert az új fázis képződésével járó heterogén kémiai folyamatok oszcillációs viselkedése is. Ostwald (1900) figyelte meg például a hidrogén képződési sebességének periodicitását a króm sósavas oldódása során. Sokan tanulmányozták a termokémiai oszcillációkat is. Ezek egyik legismertebb példája az ún. hideglángok jelensége: alkánok és hasonló anyagok alacsony hőmérsékletű (kb. 400 oC) tökéletlen égésekor szabályos időközönként egy lassan mozgó, halványkék láng jelenik meg a reakciótérben (Frank-Kamenyeckij, 1943).
A kémiai folyamatokhoz kapcsolódó fizikai folyamatok szerepét a periodikus viselkedés kialakulásában annyira nélkülözhetetlennek vélték, hogy a mai tudásunk szerint legrégebben felfedezett homogén, izoterm körülmények között és oldatfázisban lejátszódó oszcillációs reakció, az ún. Bray–Liebhafsky–reakció (Bray, 1921, 1931) értelmezésével kapcsolatban sokáig tartotta magát az az elképzelés, hogy az oszcilláció eredete különböző heterogenitásokban keresendő.
A homogén oszcillációs reakciók kutatásában
az igazi áttörést a véletlenül felfedezett Belouszov–Zsabotyinszkij
(BZ)–reakció mechanizmusának felderítése jelentette. Belouszov
(1959) figyelte meg először, hogy a citromsav kénsavas közegbeli
és Ce(IV)/Ce(III)-ionokkal katalizált bromátos oxidációja során az oldat
színe a katalizátor oxidált és redukált állapotára jellemző
sárga
és
színtelen
állapotok
között hosszantartóan oszcillál. A reakciót később
Zsabotyinszkij
(1964) tanulmányozta alaposabban, és megalkotta az oszcilláló rendszer
első elvi sémáját is.
A reakciónak ma számos változata ismert. Ezek közül a legtöbbször alkalmazott az, amelyben a citromsavat malonsavval helyettesítjük. A szakirodalom ma ezt a rendszert nevezi BZ–reakciónak. Az oszcilláció eredetét értelmező reakciómechanizmust Field, Kőrös és Noyes (FKN) dolgozta ki (Field, 1972). Az FKN–elmélet sikere bizonyította, hogy oszcilláció csak kémiai folyamatok eredményeként is kialakulhat.
Több ezerre tehető a témakörben az elmúlt 30 évben megjelent közlemények száma. A kutatások kezdeti szakaszának eredményeiről gazdagon tájékoztat a Field és Burger (1985) által szerkesztett könyv, a későbbiekben elért eredményekről pedig részletes összefoglaló olvasható Scott (1993) valamint Gray és Scott (1994) könyvében.
Az értekezésben összefoglalt közleményekben a BZ–reakció központi szerepet tölt be. Ebben a rendszerben szabályoztunk először kémiai káoszt [3], s a BZ–elegyben vizsgáltuk a kémiai hullámok terjedésének és csatolásának törvényszerűségeit is [1, 2, 4, 5, 7, 8]. Indokolt tehát, hogy rövid magyarázatát adjam a BZ–rendszer egzotikus viselkedésének.
Talán meglepő, de a reakció mechanizmusának minden részlete még ma sem ismert. A legrészletesebb mechanizmust, amely 26 részecskét és 80 elemi reakciólépést (!) tartalmaz, Györgyi, Turányi és Field (1990) közölte. A közlemény „Abstract”-jának utolsó mondata így szól: „Several areas in need of further work are identified”. A problémát a cérium(IV)-ion és a malonsav közötti reakció bonyolultsága okozza. A legkorszerűbb HPLC–berendezések alkalmazásával végzett legújabb kutatások, melyeket Noszticzius és Försterling irányítottak, számos új részlettel gazdagították a reakcióval kapcsolatos ismereteinket (Oslonovitch, 1998; Hegedűs, 2000).
A BZ–reakció bonyolultsága a témakört nem ismerő olvasóban azt a jogos képzetet keltheti, hogy az oszcilláció oka – minden bizonnyal – a reakciómechanizmus szinte kiismerhetetlen gazdagsága. Field és Noyes azonban megmutatta (Field, 1974a), hogy az FKN–mechanizmusból levezethető egy egyszerű vázmodell – az ún. Oregonátor-modell–, melynek segítségével az oszcilláció kialakulása könnyen értelmezhető.
Az Oregonátor-modell a következő reakciólépéseket tartalmazza:
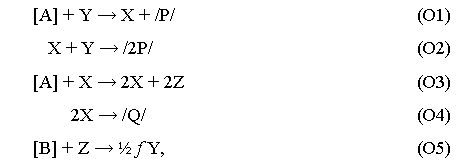
ahol [A] ş BrO3-, [B] ş oxidálható szerves molekulák, X ş HBrO2, Y ş Br-, Z ş Ce4+, /P/ és /Q/ különböző termékek, f pedig egy ún. sztöchiometriai állandó. A szögletes zárójel az adott komponens nagy feleslegét jelzi.
A modell alapján az oszcilláció kialakulása a következőképpen magyarázható: a kis koncentrációban lévő köztitermékek, a brómossav (X) és a bromidion (Y) „versenyeznek” a nagy feleslegben lévő bromátionnal (A) való reakcióért. A versengő köztitermékek azonban egyszerre nem lehetnek jelen nagy mennyiségben, mert a rendkívül gyors (O2) reakcióban egymással reagálnak. Amikor viszont a bromidion koncentrációja kicsi, akkor a brómossav mennyisége az (O3) reakcióban autokatalitikusan növekedhet. Ennek eredményeként a cérium(IV)-ion (Z) koncentrációjának növekedése is felgyorsul, aminek hatására viszont az (O5) reakcióban kis késleltetéssel ugyan, de a bromidion is egyre nagyobb mennyiségben képződik. Így az autokatalitikus folyamat előbb-utóbb leáll, s a brómossav az (O4) reakcióban elfogy. Az autokatalitikus (O3) reakció csak akkor indulhat el újra, amikor az (O1)–(O2) reakciók együttes hatására a bromidion koncentrációja ismét egy kritikus szint alá csökken. S ekkor minden kezdődik előről… Röviden azt mondhatjuk, hogy a BZ–reakció oszcillációs viselkedése az autokatalízis és a késleltetett negatív visszacsatolás (inhibíció) együttes hatásával magyarázható.
Az Oregonátor-modellből könnyen levezethető egy kétváltozós, csak dimenziómentes mennyiségeket tartalmazó differenciálegyenlet-rendszer:
![]() (2.1)
(2.1)
![]() (2.2)
(2.2)
amelyet Tyson–Fife–modellnek nevezünk (Tyson, 1980).
A (2.1)–(2.2) egyenletekben x
és
z
a megfelelő komponensek dimenziómentes koncentrációja,
t
a
dimenziómentes idő, e
és
q
pedig dimenziómentes állandók. Ez a modell sokszor szerepel az értekezésben
összefoglalt közleményekben is. Haszna a következő: egy adott stacionárius
(egyensúlyi) megoldáshoz tartozó ![]() és
és ![]() értékek egy pontot (stacionárius pont) jelölnek ki a változók fázisterében
(z vs x). Egy stacionárius pont stabilitásának jellemzésére
pedig ún. lineáris stabilitásvizsgálatot végezhetünk.
értékek egy pontot (stacionárius pont) jelölnek ki a változók fázisterében
(z vs x). Egy stacionárius pont stabilitásának jellemzésére
pedig ún. lineáris stabilitásvizsgálatot végezhetünk.
Ennek lényege röviden a következő.
Tekintsük az n dinamikai változó n-dimenziós fázisterének
egy tetszőleges fázispontját az ![]() stacionárius pont kicsiny környezetében. Tételezzük fel, hogy a fázispont
stacionárius pont kicsiny környezetében. Tételezzük fel, hogy a fázispont ![]() koordinátáinak értéke a
koordinátáinak értéke a ![]() időpontban
egyszerű exponenciális függvényekkel számítható:
időpontban
egyszerű exponenciális függvényekkel számítható:
![]() ,
(2.3)
,
(2.3)
ahol ![]() ,
via
kezdeti feltételektől függő állandó és l
a stacionárius pont ún. sajátértéke. Ennek kiszámításához állítsuk
elő a vizsgált rendszer dinamikáját leíró differenciálegyenlet-rendszer:
,
via
kezdeti feltételektől függő állandó és l
a stacionárius pont ún. sajátértéke. Ennek kiszámításához állítsuk
elő a vizsgált rendszer dinamikáját leíró differenciálegyenlet-rendszer:
![]() ,
(2.4)
,
(2.4)
ún. Jacobi–mátrixát (J) az ![]() stacionárius pontban:
stacionárius pontban:
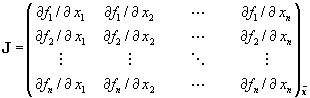 .
(2.5)
.
(2.5)
Tételezzük fel, hogy egy fázispont helyzetének változása a stacionárius pont kicsiny környezetében jó közelítéssel leírható a differenciálegyenlet-rendszer ún. linearizált alakjával:
![]() ,
(2.6)
,
(2.6)
ahol![]() .
Ekkor a (2.3) egyenleteket behelyettesítve a (2.6) egyenletbe az adódik,
hogy
.
Ekkor a (2.3) egyenleteket behelyettesítve a (2.6) egyenletbe az adódik,
hogy
![]() ,
(2.7)
,
(2.7)
ahol I az egységmátrix, ![]() a
l
sajátértékhez tartozó ún. sajátvektor, 0 pedig egy – csak
nullákat tartalmazó – oszlopvektor. Ha v ±
0
akkor (2.7) csak úgy teljesülhet, ha
a
l
sajátértékhez tartozó ún. sajátvektor, 0 pedig egy – csak
nullákat tartalmazó – oszlopvektor. Ha v ±
0
akkor (2.7) csak úgy teljesülhet, ha
![]() .
(2.8)
.
(2.8)
A (2.8)-ból adódó ún. karakterisztikus-egyenletnek
(a l -ra n-edfokú polinomnak) n darab gyöke van ![]() ,
s így egy fázispont koordinátáinak időbeli változását leíró teljesen általános
megoldás a lineárisan független megoldások lineáris kombinációja:
,
s így egy fázispont koordinátáinak időbeli változását leíró teljesen általános
megoldás a lineárisan független megoldások lineáris kombinációja:
![]() ,
(2.9)
,
(2.9)
ahol cj a kezdeti feltételektől függő állandó. A stacionárius pont stabilitását a sajátértékek vizsgálata alapján jellemezhetjük. Egy sajátérték valós vagy komplex szám, de a stabilitás szempontjából elegendő a komplex szám valós részének előjelét vizsgálni. Ha az összes sajátérték valós része negatív, akkor a stacionárius pont stabilis, mert a (2.9) egyenlet értelmében a fázispont időben egyre közelebb kerül a stacionárius ponthoz. Ezzel ellentétben, ha van legalább egy olyan sajátérték, amelynek valós része pozitív, akkor a stacionárius pont instabilis. Ekkor ugyanis a pozitív sajátértékhez tartozó sajátvektor irányában a fázispont mindig távolodni fog a stacionárius ponttól.
Az Oregonátor-modellben szereplő f sztöchiometriai állandó értékének változtatásával végzett számítások eredményei azt mutatták, hogy a (2.1)–(2.2) egyenletekkel leírt dinamikai rendszernek háromféle stacionárius állapota lehet (Tyson, 1980):
A kémiai hullámok vizsgálata során nagyon gyakran egy ismert redoxiindikátort, [trisz(1,10-o-fenantrolin)-ferrát(II)]-szulfát komplexet adunk a BZ–elegyhez. Mivel a redukált alak (ferroin) színe élénk piros, az oxidált alaké (ferriin) pedig halványkék, a folyamatokkal járó színváltozást sokkal jobban láthatjuk. Régóta ismert, hogy a ferroin önmagában is képes „katalizálni” a BZ–reakciót (Vavilin, 1969). A ferroin-katalizálta rendszerek mechanizmusa azonban sokkal bonyolultabb, mint a cériumionok-katalizálta rendszereké. Erre utaltak az ún. ferroin-katalizálta bromát-oszcillátor (ferroin–bromát–bromid CSTR-beli rendszer) dinamikájával kapcsolatos korábbi megfigyeléseink is (Gáspár, 1985), amelyeket később a 2.1 táblázatban látható mechanizmussal értelmeztünk [14].
2.1 táblázat: A
ferroin-katalizálta bromát-oszcillátor mechanizmusa [14]
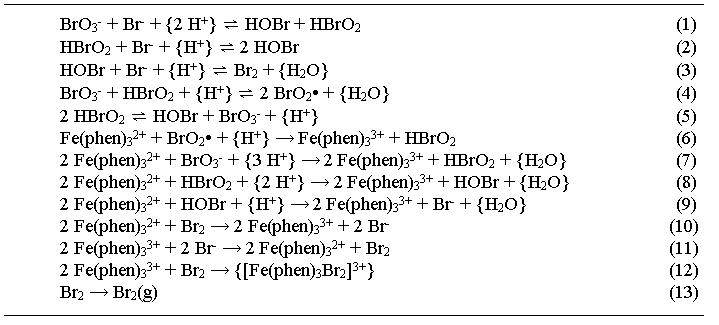
A { }-ben szereplő
részecskék koncentrációját a modellszámításokban állandónak tekintettük.phen
= 1,10-o-fenantrolin.
Mivel a kémiai hullámok vizsgálatakor nagy feleslegben alkalmazunk malonsavat, a ferroin-katalizálta minimális bromát-oszcillátor komplexitását okozó (7)–(13) reakciólépések hatását a [ferriin]/[ferroin] arány alakulására elhanyagolhatjuk a ferriin–malonsav reakció hatásához képest. Ez utóbbi reakció azonban jól leírható (sematikusan) az Oregonátor-modell (O5) lépésével. Így, habár tudjuk, hogy a ferroin-katalizálta rendszerek mechanizmusa sokkal bonyolultabb, mint a cériumionok-katalizálta rendszereké, az egyszerű Tyson–Fife–modellt a ferroin-katalizálta BZ–rendszerekre is jól alkalmazható közelítésnek tekintjük.
Kémiai oszcilláció nem csak a BZ–reakcióban megismert módon (az autokatalízis és a késleltetett negatív visszacsatolás összekapcsolásával) jöhet létre. Jól ismertek olyan reakciósémák is, amelyekben az oszcilláció megjelenése sokkal egyszerűbb okokra vezethető vissza. A legismertebb klasszikus példa a Lotka–Volterra (LV)–modell (Lotka, 1920; Volterra, 1931):


Ebben a sémában, amely már határciklusos oszcillációt mutat, az oszcilláció eredete az autokatalitikus (A3) reakció és a felszaporodó részecskét fogyasztó elsőrendű (A4) reakció versengése. Az első két reakció a ciklus újraindulását biztosítja.
Nagyon hasonló az Autokatalátor-modellhez az Edblom, Orbán és Epstein (EOE) által 1986-ban felfedezett első CSTR-beli pH–oszcillációs reakció, a jodát–szulfit–ferrocianid-rendszer vázmodellje (Gáspár és Showalter, 1987, 1990):

ahol [A] ş SO32-, X ş HSO3-, Y ş H+ és Z ş I2. A hasonlóság különösen akkor szembetűnő, ha a (GS3) és (GS4) lépéseket kombinálva egy kétváltozós (X és Y) rendszert hozunk létre, amelyben Z értékét steady-state közelítéssel számítjuk a változók pillanatnyi értéke alapján. Az EOE–reakciót tehát az Autokatalátor-modell kémiai megvalósításának is tekinthetjük. A (GS1) folyamat egyensúlyi jellege miatt azonban az EOE–reakció csak CSTR-ben oszcillál.
Rábai és Beck (1988) egy Landolt–reakció perturbálásával olyan pH–oszcillátort hozott létre, amely zárt reaktorban és CSTR-ben is oszcillál. A jodát–szulfit–tioszulfát- rendszer oszcillációs viselkedését a következő modellel értelmezték:
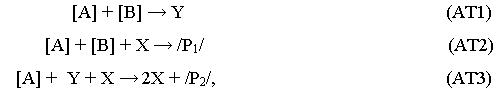
melyben [A ] ş IO3-, [B] ş S2O32-, X ş H+, Y ş HSO3-, /P1/ ş S4O62- és /P2/ ş SO42-. Az oszcilláció eredete ebben a reakciósémában, amelyet a szerzők Alternátornak neveztek el, az (AT3) és (AT2) reakciólépések váltakozása. A ciklus első szakaszában X autokatalitikusan szaporodik, a második szakaszban pedig pszeudo elsőrendű kinetika szerint fogy.
Rábai legújabban (1998) egy olyan egyszerű reakciósémát közölt, amelynek alapján könnyen tervezhetők pH–oszcillációs reakciók:
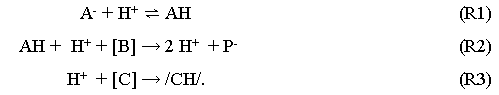
A Rábai–modellben felismerhetjük
a GS–modell első lépését (gyors protonálódási egyensúly) és az Alternátor
váltakozó reakcióit: a köztitermék (H+) koncentrációjának autokatalitikus
növekedését és egyszerű kinetika szerinti csökkenését. A hidrogén-peroxid–
szulfit–hidrogén-karbonát-rendszer
CSTR-beli oszcillációja (Rábai,
1997) ezzel az egyszerű modellel írható le.
Az egyszerű reakciósémák bemutatásával azt kívántam bizonyítani, hogy a kémiai oszcilláció – a jelenség lényegét tekintve – igen egyszerű okokra vezethető vissza. Beck (1992) fogalmazta meg az egyik legérdekesebb kérdést. Ha kémiai oszcilláció ilyen egyszerűen kialakulhat, akkor miért van mégis olyan kevés oszcilláló reakció? Az oszcilláció szükséges és elégséges feltételeinek szisztematikus vizsgálatával arra a következtetésre jutott, hogy bár a reakciómechanizmus alapján számos redoxireakció lehetne periodikus, azonban az elemi lépések sebességi együtthatói olyanok, hogy az oszcilláció kialakulásának parametrikus feltételei a legtöbb esetben nem teljesülnek.
A bonyolult, sok kémiai komponenst
tartalmazó kísérleti rendszerekben tapasztalt oszcilláció értelmezésére
kidolgozott egyszerű modellek előnye, hogy ezekre könnyen alkalmazhatók
a bifurkációs elmélet matematikai módszerei. Az oszcillációra vezető bifurkációknak
több módozata is ismert (Maselko,
1982). Például, a BZ–rendszer dinamikáját leíró Tyson–Fife–modellben
az oszcilláció ún. Hopf–bifurkációval jön létre. Erre az jellemző,
hogy a bifurkációs paraméter egy kritikus értékénél a stabilis stacionárius
pont sajátértékének valós része negatívból zérussá válik, miközben a képzetes
rész nem nulla. A paraméter értékének további változtatásakor azonban a
stacionárius pont instabilissá válik (sajátértékének valós része pozitív
lesz), s egy új stabilis attraktor (vonzó pontok halmaza), az instabilis
stacionárius pontot körbevevő stabilis határciklus jelenik meg a
változók fázisterében. A következő alfejezetben
azt is megmutatom, hogy a kémiai káosz kialakulása hasonlóképpen könnyen
értelmezhető a bifurkációs elmélet segítségével.